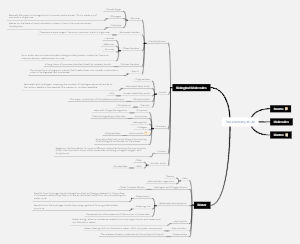
MindMap Gallery Operación en estado no estacionario para reactores con agitación
Operación en estado no estacionario para reactores con agitación
Descripción de ecuaciones empleadas en reactores con operación enestado no estacionario.
Edited at 2021-07-19 22:23:11Operación en estado no estacionario para reactores con agitación
- Recommended to you
- Outline