MindMap Gallery Velocidades iniciales y vida media
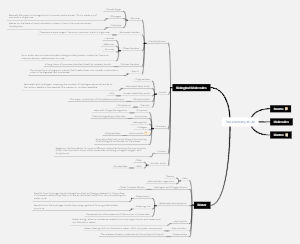
Velocidades iniciales y vida media
Secuencia de las velocidades iniciales y el tiempo de vida media de una reacción.
Edited at 2021-07-26 22:27:08Velocidades iniciales y vida media
- Recommended to you
- Outline